あくまでも、世の中にある知識を基にした私の推論であることを、予めご了承ください。
事実関係を確認していないので、間違っているかもしれません。
赤道は低気圧とのことですが、どのようにして低気圧になっているか、私なりに分析したいと思います。

まず、地球は反時計回りに回転しています。
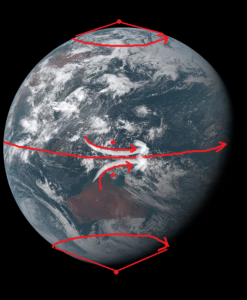
極では冷たく重い水、冷たく重い大気、比較的軽い成層圏の大気があります。
冷たく比重の重い水や大気は圧力が強く、冬の成層圏は太陽の光を受けないので寒く、夏の成層圏は太陽の光を受け続けるため高温になります。
温かく軽い大気は上昇気流を生み低気圧になり、冷たい大気は重く下降気流を生み高気圧になります。

赤道へ目を向けると、地球の中心は西から東へ回転しています。
北半球と南半球で、低気圧の回転は逆となりますので、赤道からやや北、赤道からやや南へ中心点を置き地球を回転させると、北では反時計回りの回転、南では時計回りの回転、つまり低気圧性の回転が起こっていると言えます。

中心が低気圧ということは、周囲から高気圧性の風、北半球では時計回りの風、南半球では反時計回りの風が吹き込みます。
これが赤道付近を流れる東風、貿易風と呼ばれます。
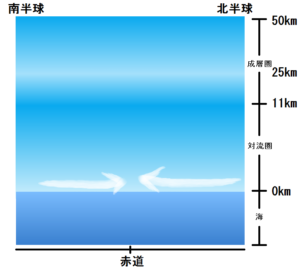
赤道へは、北半球と南半球から低気圧へ風が吹きます。
2018-09-55.png
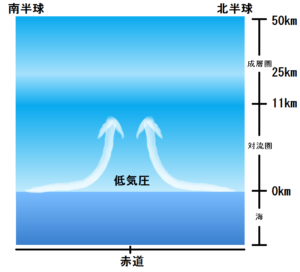
北半球から赤道への風、南半球から北への風がぶつかると、下には重い海水がありますので上空へと風は逃げていきます。
この様に、低気圧性の対流が生まれているように思えます。
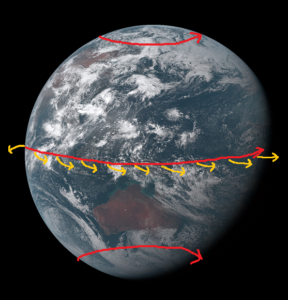
さて、何故赤道方向へ風が流れ上昇気流になるか考えますと、図を見てわかる通り地球は回転しています。
地球は物質で、この物質へ回転による遠心力が働いています。
つまり、赤道は地球の中心から働く遠心力により、宇宙へ向かう力が働いているため、上昇気流が生じるのではないかと思います。
以上、物理的な観点から分析してみました。
———————————————————————————————-
時間を置いて再度見直し
台風の構造
あくまでも、世の中にある知識を基にした私の推論であることを、予めご了承ください。
事実関係を確認していないので、間違っているかもしれません。
今回は、台風の構造を分析したいと思います。
発生時の特徴を挙げます。
詳しい発生原因は分かりません。(^^)
1.通常、日本の夏(熱赤道が日本の南)にあるとき発生し易い。
2.大気が安定しているときに発生しているように思える。
3.海水温25度以上で発生すると言われています。
2018-09-10a.png
大気が不安定な場合に発生し難い理由を説明しますと、まず風呂で手を使い水面に渦を作る場面を想像してください。
水面が波立っているときは渦が出来にくく、水面が波立っていないときは渦ができ易い。
大気も同じで、大気が安定しているときは渦ができ易く、大気が不安定なときは渦ができ難い。
2018-09-11a.png
熱帯で発生する熱帯低気圧が台風になるのですが、台風発生地点は海水温が25度と高く、高い海水温上では湿気を含んだ上昇気流が生まれます。
海面付近では、上昇気流により大気が上へ引っ張られ気圧が低下します。
2018-09-11b.png
気圧が低下すると周囲から風が集まり、高気圧と低気圧による対流が生じます。
徐々に反時計回りの渦が出来、雲が集まります。
2018-09-12.png
高い海水温により上昇気流が勢いづいていき、更に気圧が低下。
風量が増し、台風となります。
さて、ここまでは普通の話で、これだけならば、私が苦労して絵を描き説明する必要はありません。(^^;
ここからが本題です。
2018-09-13.png
通常、台風は熱帯で発生します。
台風内は、次のような状態だと思います。
1.25度以上の海水が常に供給される。
2.気圧が低下することで、周囲より気温が低下している。
3.雲が太陽光を遮断することにより気温が下がる。
4.気温が下がると、更に気圧が低下する。
2018-09-14.png
#図は、台風時の温度差を表しています。
雲が日射を受けるのですが、日射を受けた雲は更に気化し膨張します。
つまり、台風上部の大気は膨張するため、対流圏と成層圏の境目では膨張により気圧が高くなるのではないかと思います。
2018-09-15.png
その為、台風内は気圧が低く反時計回りに大気が回転し、台風の雲より上では気圧が高く時計回りに大気が回転します。
高気圧と低気圧の境目では、対流により風が衝突し、雲が出来易いのかもしれません。
台風内は気圧が低く強い上昇気流により上空へ昇った雲は、高気圧により台風外へ排出されます。
2018-09-16.png
その為、高気圧と低気圧の境目からは、雲が時計回りに噴出します。
図は、台風を上から見た場合、雲が時計回りに噴出している状態を描写したものです。(^^)
2018-09-17.png
台風は北上することで、高い海水温による上昇気流を得られなくなります。
2018-09-18.png
地上付近では反時計回りに風を取り込んでいますから、北西からは冷たい空気、南東からは暖かい空気を反時計回りに取り込み、温帯低気圧と化します。
2018-09-19.png
台風の経路上は台風の通過により気圧が下がるため、周囲から風や雲が集まり易くなるでしょう。
そして、台風が放出する雲の下は気温が低い。
2018-09-20.png
この経路へは、台風というきっかけにより北からは寒気が、南からは湿った暖気が衝突し、寒気と暖気がぶつかることにより上昇気流が生まれます。
雲が発達し易く、雨が降りやすいのではないかと思います。
今年、2018年7月上旬(6日ごろ)に大雨が降ったのですが(西日本豪雨)、この時の状況を説明します。
2018-09-21.png
出典:気象庁ホームページより (気象庁 海水温・海流のデータ 太平洋 旬平均海面水温)
2018-09-22.png
出典:気象庁ホームページより (気象庁 海面水温に関する診断表、データ 日別海面水温)
2018-09-23.png
1.日本南東の海水温が高く、また中国地方周辺の海水温が高く、非常に湿度が高かった。
2.冬から夏へ移り変わる頃なので、日本の北には強い寒気があった。
3.日本で最も湿度の高い梅雨に台風がやってきた。
4.台風が通ることにより台風の雲が残り、加えて経路上は低気圧化していた為、雲が集まり易く気温が低下していた。
5.台風が温帯低気圧化することにより、周囲の高気圧(オホーツク海高気圧)から冷たい風が流れ込んでいた。
6.台風の経路へ南からは非常に湿った空気、北からは冷たい空気がぶつかることにより、冷たく重い空気は下へ、軽く暖かい空気が上へ、これにより雲が発生し易い状況だった。
7.台風の発生により、台風付近の暖かい海水が日本付近へ流れ込んでいた。
この様な条件が重なり、大雨が降ったのではないかと思われます。
去年、2017年7月5日から7月6日にかけて発生した大雨(九州豪雨)についてですが、この時の状況を説明します。
2018-09-30.png
出典:気象庁ホームページより (気象庁 海面水温に関する診断表、データ 日別海面水温)
2018-09-31.png
1.ラニーニャ現象により、日本西で流れる海水の温度が高かった。
2.冬から夏へ移り変わる頃なので、日本の北には強い寒気があった。
3.日本で最も湿度の高い梅雨に台風がやってきた。
4.台風が通ることにより台風の雲が残り、加えて経路上は低気圧化していた為、雲が集まり易く気温が低下していた。
5.台風の経路へ、南からは非常に湿った空気、北からは冷たい空気がぶつかることにより、冷たく重い空気は下へ、軽く暖かい空気が上へ、これにより雲が発生し易い状況だった。
6.山の斜面に湿った空気がぶつかり空気が上昇することにより、局地的に雲が発生し易い状況だった。
7.台風の発生により、台風付近の暖かい海水が日本付近へ流れ込んでいた。
2018-09-32.png
さて、山の斜面へ風がぶつかり上昇気流が発生していたとの事ですが、図のオレンジ色の部分へかかる力を考えると、この部分は上昇気流により低気圧化していたのではないかと思います。
2018-09-33.png
上昇気流により対流が生まれ、黒い線で囲った部分が低気圧化すると、上空では左回転の渦が出来るようになります。
周囲から雲が集まり、低気圧化により気温が下がり、暖かい湿った空気は上空で冷え雲となり、雨が降ることで気温が下がり、更に雲が出来易い状態になります。
2018-09-34.png
その雲は、西から吹く風により東へ流され、東へ大雨をもたらしたというわけです。
あくまでも推論であり、事実とは異なる可能性があります。
さて、更に台風を分析したいと思います。
2018-09-40.png
台風が低い気圧を保つ場所は海面水温か高く、気圧の低下により気温が下がり、雲が日光をさえぎるため雲の下では気温が下がり、雨により気温が下がります。
2018-09-41.png
台風上部では雲が熱せられることにより大気が膨張し、中心気圧が高く(オレンジ色の部分)なると思います。
台風下部の中心気圧(黄色の部分)が低いとすると、中心気圧が低い内は下部の気圧が雲まで影響を与えないでしょう。
2018-09-42.png
更に台風の気圧が下がると、気圧の低い場所が上部、つまり雲が有る部分まで影響を与えるようになり、目で見て分かる台風の目が現れるのではないかと思います。
台風の目がハッキリする中心部分では日光をさげぎる雲が少なくなり、台風の目では上昇気流の元となる熱が生じるように思えます。
2018-09-43.png
最近ウェザーニュースさんから耳にした情報によりますと、対流圏海面では雲が集まっているという話。
つまり、図の様な対流が説明できます。
この対流により、高気圧と低気圧の境から雲が台風の外へ流れ出していくことになります。
2018-09-44.png
もし、これらの推論が的を射ていたとすると、台風発生時は上部が高気圧、下部が低気圧になることが条件なのかもしれません。
2018-09-45.png
対流の関係を考えますと、台風の目(低気圧の中心)と上空にある高気圧の中心は多少ずれているかも知れません。
この様に妄想を膨らませてしまいます。(^^)
以上、間違いがあるかもしれませんが、分析してみました。
事実関係は確認しておりません。(^^)
———————————————————————————————-
下書き
見直し
時間を置いて再度見直し
太平洋の海流
さて、今回も世の中にある知識を基にした私の推論です。
事実関係を確認しておりません。
予めご了承ください。
2018-09-01.jpg
#日本の冬を例にしています。
通常、赤道に日光が当たるので、海が動かない場合、図の様に気温が上がります。
2018-09-02.jpg
ここへ図の様な海流が加わると、赤道で温められた水が移動するわけです。
2018-09-03.png
すると、図の様に暖かい海水が西へ移動します。
その為、太平洋西は温暖化の影響を受けやすいと思います。
次は、各地の海流を更に細かく分析したいと思います。
2018-09-04.png
北から冷たい海水が流入するBとDは、暖かい海水は海面へ、冷たい海水は水中へ移動するのではないかと思います。
Aの部分は、北と南から冷たい海流がぶつかる部分で、図の様に見ると狭い範囲と思いますが、実物の海では数百キロの範囲に北と南から冷たい海水が衝突することになります。
その一部は、東から西へ流れ、一部は衝突により溜まるのかも知れません。
Cの部分は、東から流れてきた海面の暖かい海水と海中の冷たい海水が、一部は南北へ流れ、一部は行き場を失う場所のように思えます。
2018-09-03.png
図を見て分かるとおり、温暖化になる事により、太平洋西は比較的温暖化の影響を受けやすく、太平洋東は比較的温暖化の影響を受け難いことが分かります。
温暖化により海水が温められているので、水蒸気により湿度が上昇し、雲が出来やすく、雨が降るというわけです。
南日本周辺に暖かい海水が集まっています。
今年の蒸し暑さは、この海水温によるものだと思います。
編集中。
